HTML
-
不同品种的小麦在抗虫病害、质量、产量等方面表现出不同的特性,高品质的小麦种子在小麦产量和质量的提高中起着至关重要的作用,种子混杂时将给育种、种植和商品质量带来巨大的经济损失。随着现代种业中大量种子的不断流通,很可能造成不同品种小麦种子在运输、储存和生产过程中意外混合,必然会降低小麦品质和产量[1]。连续几年的中央一号文件都将种业发展提升到国家粮食战略上,在培育优质小麦种子的同时,对种子纯度进行鉴别成为了科研工作者迫切的任务,因此,种子纯度也成为了《农作物种子检验规程》的必检项目。
近10年来,随着具有快速、无损的高光谱成像技术的发展,越来越多的科研工作者将高光谱成像技术应用到农作物种子研究上,并取得了良好的成果[2-4]。但是, 当前基于高光谱成像技术对小麦种子进行纯度鉴别或分类的许多研究都是假设正负样本数量是一致的[1, 5-6],文中正样本指待检测出的所需品种小麦种子,负样本指混入的其它杂质品种小麦种子。然而当面临实际检测时,由于杂质负样本数量少于正样本数量的情况会导致利用传统算法时分类结果倾向于多数类,而使少数类的分类效果降低[7]。同时,相较于多光谱而言,高光谱图像含有的信息较多,相邻波段间的冗余信息高度相关,还有可能携带无助于判别的噪声信息,因此这也会在一定程度上影响模型纯度检测性能[8-9]。
为了减小样本不均衡造成的纯度检测精度低的影响,本文作者采用合成少数类过采样技术(synthetic minority oversampling technique, SMOTE)对小麦种子的杂质负样本进行扩充,使正负样本数量保持一致,为了消除波段间存在的冗余信息,进一步提高模型的检测精度,再采用非信息变量去除(uninformative variable elimination, UVE)进行波段选择,最后采用支持向量机(support vector machines, SVM)作为分类器。为了更好地比较模型性能,在波段选择算法上对比了连续投影算法(successive projections algorithm, SPA),在分类算法上分别对比了支持向量数据描述(support vector data description, SVDD)和k最近邻(k-nearest neighbor, KNN)算法,结果表明,所提方法在所有比较的方法中效果最好。
-
实验中采用由5个品种的小麦种子(中化现代农业有限公司,中国北京),分别为JM22(济麦22,山东)、JM44(济麦44,山东)、XM26(新麦26,河南)、BN4199(百农4199,河南)和ZM33(周麦33,河南)各1000粒,共5000粒。按照面筋数值划分可分为强筋和中筋,详细信息如表 1所示,杂交时的父本和母本在表中用亲缘关系表示。
variety origin place kinship gluten value JM22 Shandong 935024/935106 medium gluten XM26 Henan Xinmai9408/Jinan17 strong gluten JM44 Shandong 954072/Jinan17 strong gluten BN4199 Henan Bainonggaoguang3709F2/BainongAK58 medium gluten ZM33 Henan Zhengmai366/BainongAK58 strong gluten Table 1. Details of 5 varieties of wheat
-
实验中使用的高光谱采集系统主要由高光谱相机、载物台及其移动平台、光源组成。高光谱相机采集的光谱范围为400 nm~1000 nm、光谱分辨率为1.29 nm、波段间隔为0.64 nm,空间像素合并值设置为10,采用150 W的光纤卤素灯作为光源,其它参数等详细介绍见参考文献[10]。在进行图像采集时,设置高光谱相机的曝光时间设置为0.25 s,光源功率设置为60 W,图像采集采用线扫描的方式,所采集的高光谱图像合计扫描1000条线,每条线在2维平面上含有1392个像素点,每个像素点采集的是94个不同的光谱波段,因而所采集到的高光谱图像3维大小为[1000, 1392, 94]。由于黑色数粒板能够防止小麦种子移动过程中出现晃动以及对采集的图像进行预处理时易于分割的特点,因而在采集过程中将每个品种的小麦分为10个批次,每个批次100粒小麦种子样本放置在黑色数粒板上,这样5个品种的小麦将会得到50幅小麦种子的高光谱图像,实际上相机捕获的高光谱数据是通过光源照射到样本再反射到相机的反射率获得的,因而光谱数据也可以称为光谱反射率[11]。本文中选取了各品种小麦任一批次下的高光谱图像,并通过ENVI 4.3选择RGB对应的3个波段的数据组成的伪彩色图像,如图 1所示。从图像也可以看出,不同品种小麦的形状、外观等特征较为接近,几乎无法通过肉眼识别。
-
实验中采集的高光谱图像中除小麦种子样品有效的高光谱信息外,还有背景板信息以及电荷耦合器件(chang-coupled device, CCD)中含有的电流暗噪声等多种信息,尤其电流暗噪声信息会对结果分析产生较大影响,因而首先要对采集到的图像进行校正,校正公式如下:
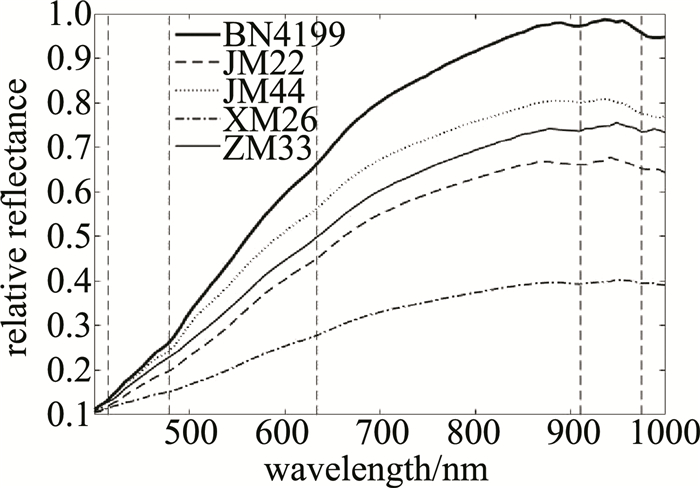
式中:Iraw、Iwhite、Iblack和I分别为通过相机采集到的原始高光谱图像、标准白板下的高光谱图像、标准黑板下的高光谱图像和校正后的图像。完成黑白板校正后,需要进一步提取小麦种子所在区域内(也称为感兴趣区域)的有效信息,该有效信息是利用阈值分割算法(阈值分割-腐蚀膨胀-计算均值光谱信息)进行提取的。完成上述步骤后,即可得到小麦种子的均值光谱信息,将每粒小麦种子的均值光谱作为模型的输入特征,各品种小麦种子中的平均光谱曲线(反射率)如图 2所示。图中垂直虚线所在位置为各品种小麦的吸收峰在波段的分布。表 2中给出了吸收峰所处的波段范围以及影响吸收峰的因素。结合图 2和表 2可知,品种为BN4199的小麦种子反射率较高,品种为XM26的小麦种子反射率较低,与其它品种小麦的光谱曲线差异较为明显,其余3类品种小麦种子的光谱曲线较为接近,这些差异主要是由于小麦种子中蛋白质、淀粉和水的成分含量不同造成的。
1.1. 实验材料
1.2. 样本采集与预处理
1.2.1. 样本采集
1.2.2. 高光谱图像预处理
-
由于过采样技术只是对样本进行简单机械地复制,并不能引入新的有效信息,因而往往不会提升模型的分类效果,还可能造成过拟合的风险[15]。为了提升模型的分类效果并降低过采样技术中过拟合的风险,本文作者提出了将SMOTE应用到不均衡样本的小麦种子纯度检测中,使正负样本的数量一致。SMOTE合成样本的策略是对负样本所在类中的每一个样本m,从其邻近的若干样本中随机选择P个样本mi(i=1, 2, …, P),然后从m和每一个mi之间合成一个新的样本mnew,样本合成公式如下所示:
式中:rand(0, 1)表示0~1范围内的随机数。
-
与多光谱图像相比,高光谱图像数据的波段数目较多,相邻波段信息高度相关,因而可能携带无助于判别的冗余信息[16-17]。为了消除波段间的冗余信息,并尽可能地提高模型的分类精度,本文中在对杂质负样本进行扩充后,对光谱波段进行选择。UVE的基本思想是通过建立偏最小二乘(partial least squares, PLS)模型去除与信息判别无关的波长,选出特征波长,被去除的波长也称为无信息变量[18],假设原始样本矩阵为样本矩阵,记为XM×N,样本标签记为yM×1,其中M为样本个数,N为波段数目,算法步骤见下。
(a) 以最低均方根误差预测(root-mean-square error of prediction,RMSEP)RRMSEP为准则[18]确定最优模型复杂度,如下式所示:
式中:yi为样本标签; $ \hat{y}_{i}$为预测值; i=1, 2, 3, …, M。
(b) 生成M×N维噪声矩阵RM×N,将原始矩阵与噪声矩阵组成新的矩阵,记为SM×2N,SM×2N=[XM×N, RM×N]。
(c) 根据留一交叉验证确定回归系数矩阵AM×2N,将AM×2N中的元素记为aij,其中i=1, 2, 3, …, M; j=1, 2, 3, …, 2N。
(d) 确定各列向量平均值 aj、标准差s(aj)以及回归系数平均值与标准差的比值,记为cj,j=1, 2, 3, …, 2N。
(e) 在XM×N中消除abs(cj)小于某一阈值的实验变量,j=1, 2, 3, …, 2N,得到新的矩阵Xnew,建立最终留一交叉验证模型,并对样本矩阵进行预测,得到新的RRMSEP,记为RRMSEPN。
(f) 分析RRMSEPN,若RRMSEPN>RRMSEP, 则重设噪声参数,进入步骤(b)循环,否则输出光谱特征变量。
-
本文中采用SVM作为分类器。线性SVM的基本原理为:寻求建立一个几何间隔最大的超球面, 使正样本数据尽可能地分布在该超球面内,而负样本数据分布在超球面外。然而, 当面临例如小麦种子纯度检测这类低维线性不可分的问题时,则无法通过线性SVM进行求解。CORTES等人[19]将核函数引入SVM中,通过非线性变换将该低维数据转变为高维数据,从而实现其线性可分。因而自其提出以来, 在许多领域受到了较为广泛的应用, 并取得了良好效果[20-22]。根据SVM的原理,构建的超平面应为:
式中: w表示平面的法向量; b表示偏移量。为了使训练数据集{x|xi ∈ RN, i=1, 2, …, M}(其中xi是1×N维的向量,RN是实数集)和yi∈{+1, -1}能够正确分类,则应满足:
式中: sign(·)是符号函数; Ω(x)为非线性映射。则最终构建的SVM优化函数及其约束条件为:
式中:J(w, ei)表示目标函数; ‖w‖表示w的F范数; φ(xi)表示非线性函数; ei为误差变量,i=1, 2, …, M;γ为惩罚因子, 其求解过程转化为朗格朗日的对偶问题,最终求得:
式中:αi是拉格朗日系数;Q(x, xi)为核函数,通常采用径向基核函数,其公式如下:
式中:σ2为方差。
-
本文中采用准确率、精确率以及负样本的检出率t作为分类模型的评价指标,将样品分为5类:真正(true positive,TP)tTP,假正(false positive,FP)tFP,假负(false negative,FN)tFN,真负(true negative)tTN和负(negative,NEG)tNEG, 则准确率、精确率和负样本检出率的计算公式如下所示。
准确率为:
精确率为:
负样本检出率(negative detection,ND)tND为:
2.1. 合成少数类过采样技术
2.2. 非信息变量剔除算法
2.3. 支持向量机
2.4. 种子纯度评价指标
-
实验中将上述5个品种的小麦种子分为5组。第1组(JM22):正样本为JM22,负样本为XM26、JM44、BN4199和ZM33;第2组(XM26):正样本为XM26,负样本为JM22、JM44、BN4199和ZM33;第3组(JM44):正样本为JM44,负样本为JM22、XM26、BN4199和ZM33;第4组(BN4199):正样本为BN4199,负样本为JM22、XM26、JM44和ZM33;第5组(ZM33):正样本为ZM33,负样本为JM22、XM26、JM44和BN4199。
为了更好地比较不均衡样本分类模型的性能,本文中采用SVDD、KNN和SVM进行对比实验。SVDD原理参见参考文献[23],为了使建立的超球体容错能力更强,在训练的过程中,允许模型训练过程中添加少量的负样本从而使超球体更加收敛[23]。因此SVDD在许多不均衡样本与异常识别等问题具有广泛的应用[24-25]。实际上根据KNN原理(参见参考文献[26]),KNN既能够应用于在不均衡样本分类中[27-28],也可以应用于均衡样本分类[26]。因而在实验过程中将SVDD用于不均衡样本识别,KNN分别用于不均衡样本、通过SMOTE扩充后的样本以及波段选择后的样本分类识别。
实验过程中从正样本所在类随机抽取800粒、负样本每类抽取20粒共80粒分别训练SVDD模型、KNN模型和SVM模型,SVDD和SVM均采用10折交叉验证和网格寻优,KNN采用10折交叉验证和自动超参数寻优,每组随机训练10次,取其平均准确率、精确率以及负样本检出率。再从剩下的样本中,抽取200粒正样本,随机抽取负样本每类25粒共100粒作为测试集。用第2.4节中的评价指标评估各模型下测试集的结果,如表 3所示。表中最后一行为5类小麦纯度检测结果的平均值。
positive samples SVDD KNN SVM A/% P/% tND/% A/% P/% tND/% A/% P/% tND/% JM22 64.00 79.11 67.00 84.03 81.35 52.40 93.07 90.68 79.20 XM26 64.33 83.45 77.00 79.20 76.74 37.70 89.80 87.01 70.20 JM44 56.33 74.13 63.00 81.40 78.83 45.10 92.23 89.65 76.90 BN4199 62.33 87.18 85.00 82.70 80.01 49.80 95.50 84.09 87.50 ZM33 60.00 76.32 64.00 82.33 80.13 51.60 89.87 87.38 70.70 average 61.40 80.04 71.20 81.93 79.41 47.32 92.09 87.76 76.90 Table 3. Results of wheat seed purity under unbalanced samples
由表 3可知,SVDD的准确率、精确率以及负样本的检出率都较低,表明SVDD在本文中研究的不均衡样本下的小麦种子纯度检测并不适用。KNN和SVM的平均准确率和精确率都在79.00%以上,而负样本的平均检出率分别只有47.32%和76.90%,这表明利用传统算法处理不均衡样本的分类问题时会使结果倾向于多数样本类,使少数样本类的分类效果降低,负样本检出率较低,表明模型将许多负样本识别为正样本,这在小麦种子纯度检测当中的影响将是巨大的。为此,在选择上述数据集的基础上,用SMOTE算法生成一些新的负样本,使训练集中正负样本的数量均为800,分别用KNN和SVM进行评估,结果如表 4所示。
positive samples SMOTE-KNN SMOTE-SVM A/% P/% tND/% A/% P/% tND/% JM22 88.87 89.26 77.20 94.80 93.17 85.30 XM26 82.63 85.28 69.10 94.80 93.78 86.70 JM44 94.33 92.56 84.00 94.40 92.57 83.69 BN4199 88.57 89.74 78.60 96.53 95.49 90.60 ZM33 84.67 86.86 72.60 95.47 94.60 88.60 average 87.81 88.74 76.30 95.20 93.92 86.98 Table 4. Results of SMOTE seed purity after SMOTE sample extension
由表 4可知,在用SMOTE算法对不平衡样本数据集进行扩充以后,分类效果均有了显著提升,KNN模型下平均准确率从81.93%提升到了87.81%,精确率由79.41%提升到了88.74%,负样本检出率从47.32%提升到了76.30%;SVM模型下的平均准确率从92.09%提升到了95.20%,精确率由87.76%提升到了93.92%,负样本检出率从76.90%提升到了86.98%。模型在SMOTE对不平衡数据集进行扩充后负样本检测率有较大提升,这表明混有杂质品种小麦的样本被正确识别的可能性越来越大,通过SMOTE对本研究的数据集进行扩充提升分类效果是可行的。
为了尽可能地消除波段间的冗余信息,进一步提升模型的分类效果,在用SMOTE算法对数据进行扩充以后,采用UVE对波段进行选择,同时对比了SPA算法。SPA的原理参见参考文献[29]。表 5中统计了各个模型下的平均检测结果。表中最后一列是各品种小麦在SPA和UVE下的平均最佳波段数目。
model A/% P/% tND/% number SMOTE-UVE-KNN 91.12 90.09 78.50 71.00 SMOTE-SPA-KNN 90.50 89.62 77.61 74.00 SMOTE-UVE-SVM 95.98 94.94 89.32 71.00 SMOTE-SPA-SVM 95.30 94.12 87.52 74.00 Table 5. Average results of 5 wheat varieties in 4 models
由表 5可知,在保证各项评价指标不降低的前提下,用SPA和UVE选择了各品种小麦的最优波段后,SVM模型和KNN模型的分类效果均有所提升,且UVE的波段选择效果优于SPA,表明了SMOTE-UVE-SVM方法在所有比较的方法中效果最佳。表 6中给出了各品种小麦在SMOTE-UVE-SVM模型下的检测结果。由表 6可知,各品种小麦的纯度检测结果相较于SVM在全波段范围内不均衡样本的小麦种子纯度检测有较大提升,且能够保证准确率、精确率均在93.00%以上的前提下,负样本的检出率均不低于85.00%。
positive samples SMOTE-UVE-SVM A/% P/% tND/% number JM22 96.13 94.92 89.30 75.00 XM26 95.30 94.49 88.30 68.00 JM44 95.07 93.22 85.40 81.00 BN4199 97.23 96.46 92.70 72.00 ZM33 96.17 95.60 90.90 57.00 average 95.98 94.94 89.32 71.00 Table 6. Test results of 5 varieties of wheat seeds in SMOTE-UVE-SVM model
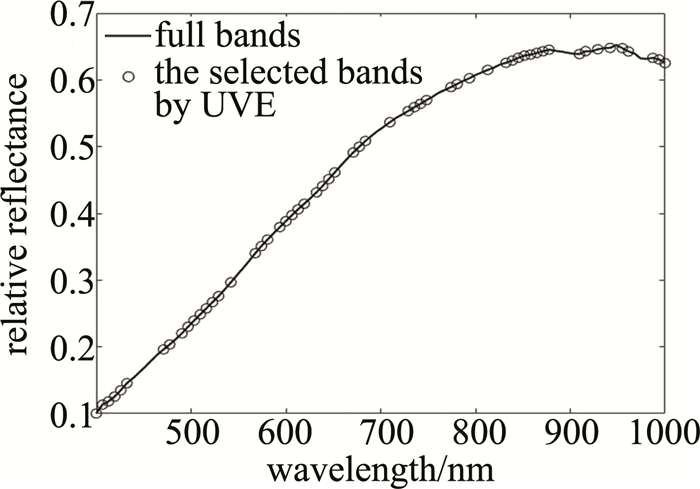
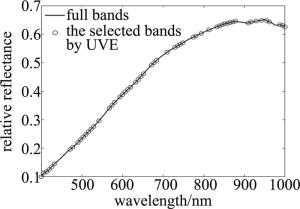
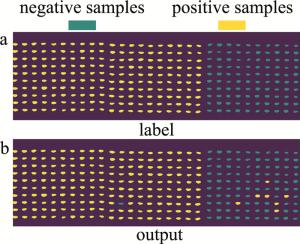
图 3中给出了UVE所选最优波段在全波段的分布。而由图 4可知,UVE所选波段除分布在除表 2所分析的吸收峰附近外,其余分布较为均匀。分析结果可知,UVE选择的波段可助于消除波段间携带的冗余信息,提升分类效果。同时本文作者选择了实验过程中以BN4199为正样本,其余品种小麦为负样本的预测结果,其准确率、精确率与负样本检出率分别为97.33%、96.60%与93.00%。图 4a和图 4b中分别给出了测试样本的标签与测试结果。
-
本文中研究了小麦种子杂质负样本不足导致纯度检测过程中模型性能偏低的问题。在运用高光谱成像技术的基础上,提出了一种基于SMOTE-UVE-SVM方法的纯度检测模型,该方法首先利用SMOTE算法对小麦种子中杂质负样本数据集扩充,使其与正样本数据的数量保持一致,再利用UVE进行波段选择,消除相同高光谱波段间可能存在的信息冗余和噪声,进一步提高小麦种子纯度检测的精度,最后用SVM进行分类。为了更好地比较模型的性能,实验过程中在均衡与不均衡样本的分类算法上分别对比了SVDD、KNN和SVM,在波段选择算法上分别对比了SPA和UVE。研究结果表明,SMOTE-UVE-SVM模型在所有比较的方法中效果最佳。由于当前仅研究了负样本中含有的4类小麦种子,在以后条件许可的情况下,应尽可能地增加负样本的类别,使模型更加具有通用性,以及能够识别出待测样本中出现未参与模型训练品种的小麦种子。

 Map
Map




 DownLoad:
DownLoad: